瘧疾是一種由原生生物瘧原蟲引起的疾病,根據世衛組織公布,全球約有一半人口身處瘧疾感染風險區,因此抗瘧疾藥物的開發,刻不容緩。
中央大學生醫理工學院院長、生命科學系教授王健家率團隊在基因研究方面取得重要突破,他們的研究為抗瘧疾藥物的開發提供新線索。研究成果並躋身國際頂尖期刊《核酸研究》(Nucleic Acids Research)。
王健家團隊發現,蘇力菌(Bacillus thuringiensis)比其他細菌多攜帶一個Prolyl-tRNA synthetase(ProRS),這個ProRS是經過基因轉移,從真核細胞轉移至細菌。然而,它的蛋白質結構在轉移過程發生改變,使其更像細菌的ProRS,對抗瘧疾藥物halofuginone(HF)產生抗性。
基因是攜帶遺傳訊息的DNA序列,經過一系列生化反應,細胞能將基因轉化為蛋白質,在這個過程aaRS(aminoacyl-tRNA synthetase)酵素會先將正確的胺基酸接到相對應的tRNA(轉運核糖核酸)分子上,再由tRNA將胺基酸運送到核醣體上進行蛋白質合成。aaRS扮演過程中關鍵酵素,如在過程中出差錯,會導致蛋白質功能異常引發多種疾病。
研究團隊指出,aaRS的結構一般來說演化時非常穩定,是ProRS的結構變異很大,細菌型和真核型ProRS有不同的tRNA偏好,無法互相替代。通常,細菌只會攜帶一個細菌型ProRS,但蘇力菌卻能同時能各帶一個細菌型與真核型ProRS。
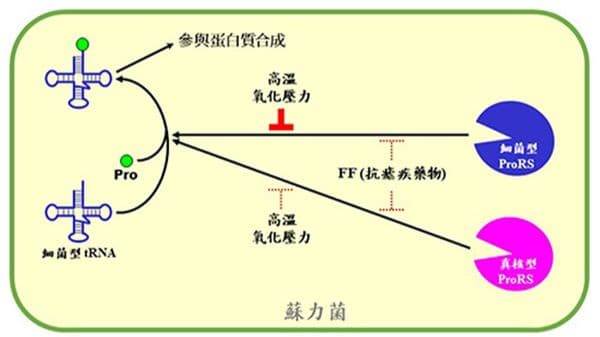
令人驚訝的是,蘇力菌的真核型ProRS在演化過程改變自身結構,使其能有效辨識細菌的tRNA,幫助蘇力菌在不同環境,如高溫和氧化壓力下生存,更重要的是,不同於其他已知的真核型ProRS,蘇力菌的真核型ProRS可以顯著提高對抗瘧疾藥物HF的耐受性。
目前,國外已有多個研究團隊正利用HF衍生藥物開發治療瘧疾、弓形蟲、隱孢子蟲等寄生生物感染的藥物。HF的結構,類似由中藥常山萃取出的一種化合物FF (febrifugine),能有效抑制瘧原蟲或其他寄生蟲的ProRS,因此被寄予厚望。
王健家與其團隊的研究為抗瘧疾藥物的研發提供新的方向和希望,團隊希望能早日將此項新線索應用在臨床治療上。
延伸閱讀
- 國衛院建立斑馬魚藥癮模式 躋身國際
- 國衛院揪自體免疫病元凶 提潛力鏢靶
- 國衛院結盟華碩 共創臺版劍橋一號
- 臺科助國泰醫院 推遠距語音篩檢醫療
- 臺科許昕 AI穿戴1分鐘快篩12慢性病
- 翻新CTC計數 臺科陳建光研發助癌療
- 感染腸病毒出現高血糖 控糖防重症
- ELECLEAN翻轉消毒史 陳建宏:給世界新選擇














